Viime aikoina on käyty laajaa keskustelua Bovaer-nimisestä rehulisäaineesta ja sen käytöstä maitotiloilla Suomessa. Ainetta käytetään vähentämään lehmien ruoansulatuksesta aiheutuvia metaanipäästöjä estämällä tiettyjen mikrobien toimintaa lehmän pötsissä. Monet kuluttajat ovat ilmaisseet huolensa aineen turvallisuudesta lehmille sekä elintarvikkeiden kautta ihmisille.
Suomessa kohu alkoi, kun paljastui, että Valio käyttää kyseistä ainetta kymmenillä maitotiloillaan. Bovaer-kohusta ovat uutisoineet muun muassa Taloussanomat ja Svenska Yle. Kyseessä on EU:n hyväksymä rehun lisäaine, jonka vaikuttava aine on 3-nitroksipropanoli (3-NOP).
Useat suomalaiset meijerit ja elintarvikeyritykset ovat ilmoittaneet, etteivät käytä tuotteissaan Bovaerilla ruokittujen lehmien maitoa tai lihaa. Valio ei ole vielä kuitenkaan reagoinut kuluttajien huoleen ja on toistaiseksi ainoastaan korostanut luottavansa aineen turvallisuuteen.
Valio perustelee luottamustaan aineeseen sillä, että “EU:n elintarvikeviranomaiset ovat todenneet aineen käytön turvalliseksi sekä lehmille että ihmisille”, ja esittää tietolähteenä myös aineen valmistajan vastineen kohuun. Monet kuluttajat ovat kyseenalaistaneet nämä perustelut ja vaativat, että Valio lopettaa aineen syöttämisen lehmille välittömästi.
Faktabaari levittää virheellisiä väitteitä Bovaer-lisäaineesta
Verkossa on liikkunut runsaasti väitteitä Bovaeria vastaan ja sen puolesta. Yksi laajalti levinnyt julkaisu on hankerahoitteisen, Avoin yhteiskunta ry:n ylläpitämän, Faktabaari-sivuston artikkeli: “Verkossa leviää virheellisiä väitteitä Bovaer-lisäaineesta.”
Faktabaarin artikkelin tarkoituksena on vakuuttaa lukijat aineen turvallisuudesta. Vaikka sen sisältö vaikuttaa ensisilmäyksellä kattavalta, se sisältää virheellisiä ja harhaanjohtavia väitteitä koskien Bovaerin vaikutuksia ja turvallisuutta ihmisille ja lehmille. Lehmät ovat olennainen osa Suomen ravintoketjua ja huoltovarmuutta, joten väitteitä on tarpeen tarkastella perusteellisesti.
Kansakunnan Tila tarjoaa perusteellisen faktantarkastuksen
Käymme tässä perusteellisessa faktantarkistuksessa läpi artikkelin 10 keskeisintä väitettä sekä arvioimme samalla Bovaerin turvallisuutta ja hyväksymisprosessia faktapohjaisesti.
Aloitamme yhteenvedolla ja käymme tämän jälkeen väitteet läpi perusteellisesti.
YHTEENVETO PERUSTEELLISESTA
FAKTANTARKISTUKSESTA
10 TARKISTETTUA VÄITETTÄ BOVAER-LISÄAINEESTA
- VÄITE 1: “Verkossa leviää virheellisiä väitteitä Bovaer-lisäaineesta.”
TARKISTUS: Totta, mutta harhaanjohtavaa.
Väitteiden virheellisyys: Bovaerista on esitetty virheellisiä tietoja, mutta monet väitteet perustuvat tieteellisiin havaintoihin. Kaikki turvallisuutta kyseenalaistavat väitteet eivät ole perusteettomia.
- VÄITE 2: “Väitteet siitä, että Bovaer olisi myrkkyä lehmille ja ihmisille, eivät ole totta.”
TARKISTUS: Väärin, harhaanjohtavaa.
Myrkyllisyys: Puhtaana aine on luokiteltu ihmiselle kohtalaisen myrkylliseksi hengitettynä sekä epäillyksi lisääntymismyrkyksi. Vaikuttava aine 3-NOP voi tutkimusten mukaan aiheuttaa vakavia terveysongelmia lehmille sekä suurilla että hyväksytyillä annoksilla.
- VÄITE 3: “Aine hajoaa märehtijän pötsissä eikä sitä siirry maitoon tai lihaan.”
TARKISTUS: Osittain väärin.
Hajoaminen: Aine hajoaa pötsissä, mutta ei täysin. Sen metaboliittia NOPA:a siirtyy verenkiertoon ja sitä on havaittu maidossa, vaikka pitoisuudet ovat alhaisia. Lisäksi aineen hiilirakenteen on havaittu siirtyvän mm. maidon laktoosiin, mutta tällä ei uskota olevan terveysvaikutuksia.
- VÄITE 4: “Lypsylehmien metaanipäästöjä vähentävä rehun lisäaine hajoaa pötsissä eikä ole tutkimusten mukaan vaarallinen.”
TARKISTUS: Väärin.
Vaarallisuus: NOPA-metaboliitti on potentiaalisesti genotoksinen ja sytotoksiseksi havaittu, jonka vaikutuksista ihmisille ei ole tietoa. Tutkimusten mukaan aineen vaikutus voi myös häiritä lehmän fysiologiaa ja aiheuttaa terveysongelmia.
- VÄITE 5: “EFSA on siis todennut Bovaerin turvalliseksi sekä lehmille että ihmisille.”
TARKISTUS: Totta, mutta harhaanjohtavaa.
Turvallisuus: EFSA:n lausunto aineen turvallisesta käyttörajasta perustuu vain kahteen tutkimukseen lehmillä. Molemmissa niistä havaittiin haittavaikutuksia ja turvallisuusmarginaalia ei voitu määrittää.
- VÄITE 6: “EU:n rehun lisäaineista annetun asetuksen mukaan eläinten ruokinnassa saa käyttää vain hyväksyttyjä rehun lisäaineita, ja 3-NOP on tällainen hyväksytty lisäaine.”
TARKISTUS: Totta.
Luokittelu: Aine on luokiteltu EU:ssa hyväksytyksi rehulisäaineeksi, mutta sen käyttö on säädeltyä. Suomessa se on hyväksytty automaattisesti EU:n kautta ilman erillistä käsittelyä.
- VÄITE 7: “Se, pääseekö rehun lisäaine hyväksyttyjen listalle, riippuu siitä, onko se turvallinen eläimille, ihmisille ja ympäristölle, ja lisäksi arvioidaan sen tehokkuutta.”
TARKISTUS: Osittain väärin.
Hyväksymisprosessi: Komission hyväksynnän perusteena käytetään EFSA:n arviointia, mutta pitkäaikaista turvallisuutta ja kaikkia riskejä ei arvioida lyhyissä tutkimuksissa.
- VÄITE 8: “Luomutuotannossa Bovaeria ei saa käyttää.”
TARKISTUS: Totta.
Luomutuotanto: Luomutuotannossa 3-NOP:n käyttö on kielletty.
- VÄITE 9: “3-NOP vähensi lehmien metaanintuotantoa myös suomalaisissa tutkimuksissa, vaikkakin vaikutus jäi pienemmäksi kuin aiemmin kerrottu 30 prosenttia.”
TARKISTUS: Totta, mutta tärkeää tietoa jätetty mainitsematta.
Tehokkuus: Metaanintuotanto väheni seosrehuruokinnassa 21-24%, mutta erillisruokinnassa vaikutus oli lyhytaikainen ja pienempi, 7-11%. Lisäksi rehunsyönti ja maidontuotanto laski.
- VÄITE 10: “Valio on vuonna 2023 kertonut, ettei pilotissa havaittu mitään muutoksia tilojen tuottaman maidon määrässä, pitoisuudessa tai laadussa.”
TARKISTUS: Osittain totta, osittain epävarmaa.
Vaikutus: Valio ilmoitti, ettei maidon määrässä tai laadussa ollut muutoksia, mutta pilottihankkeen tutkimusdataa ei ole saatavilla. Riippumattomissa tutkimuksissa on havaittu aineen alentaneen maidontuotantoa jopa -11,7% ja rehunsyöntiä -13,4% sekä muuttaneen maidon koostumusta.
PERUSTEELLINEN FAKTANTARKISTUS
10 TARKISTETTUA VÄITETTÄ BOVAER-LISÄAINEESTA
Arvioimme väitteitä enimmäkseen EFSA:n arvioimien tutkimusten perusteella, koska aineen hyväksymisprosessi EU:ssa pohjautuu niihin. Lisäksi käytämme lähteinä mm. muita arviointeja (FSA, FDA, FSCJ), saatavilla olevaa tutkimusdataa sekä kansainvälisiä arviointiohjeistuksia (OECD, EFSA, EPA).
VÄITE 1
VÄITTEIDEN VIRHEELLISYYS
“Verkossa leviää virheellisiä väitteitä Bovaer-lisäaineesta.“
TARKISTUS: Totta, mutta harhaanjohtavaa.
Faktabaarin yleisväite aiheesta on totta, mutta harhaanjohtavaa. Se, että Bovaer-lisäaineesta leviää virheellisiä tietoja verkossa pitää paikkansa. Vaikka osa väitteistä niin Bovaerin puolesta kuin vastaankin ovat liioiteltuja, monet verkossa levinneet argumentit perustuvat todellisiin tieteellisiin havaintoihin ja tutkimuksiin.
Kaikki aineen turvallisuutta kyseenalaistavat väitteet eivät suinkaan ole virheellisiä, vaikka Faktabaarin artikkelista voi saada sellaisen käsityksen.
VÄITE 2
MYRKYLLISYYS
“Väitteet siitä, että Bovaer olisi myrkkyä lehmille ja ihmisille, eivät ole totta.“
TARKISTUS: Väärin, harhaanjohtavaa.
Päivitys:
-31.1.2025 Kohtaa 2.2. (Myrkyllisyys lehmille suositusannoksella) on tarkennettu
1. Myrkyllisyys ihmisille
Bovaer voi puhtaassa muodossaan aiheuttaa ihmisille terveysriskejä, erityisesti käsittelyn aikana. Tämän totesi myös Faktabaari artikkelissaan. Artikkelissa mainitun FDA:n (Yhdysvaltain elintarvike- ja lääkevirasto) asiakirjan mukaan aine ei ole tarkoitettu ihmisille käytettäväksi. Lisäksi asiakirjassa todetaan, että aine voi vahingoittaa miesten hedelmällisyyttä ja lisääntymiselimiä sekä aiheuttaa iho- ja silmä-ärsytystä.
1.1. 3-NOP-kemikaalin luokitus
Käyttöturvallisuustiedotteesta selviää aineen tarkempi luokittelu.
- Acute Tox. 3: Akuutti myrkyllisyys, kategoria 3 (H331)
- Eye Dam. 1: Vakava silmävaurio/silmä-ärsytys, kategoria 1 (H318)
- Repr. 2: Lisääntymistoksisuus, kategoria 2 (H361f)
- Skin Irrit. 2: Ihon ärsytys, kategoria 2 (H315)
Lähde: Elanco Animal Health, Bovaer-käyttöturvallisuustiedote
Bovaerin vaikuttava aine 3-NOP on siis luokiteltu myrkylliseksi hengitettynä, vakavia silmävaurioita aiheuttavaksi, epäillyksi lisääntymiskyvylle vaaralliseksi aineeksi sekä ihoa ärsyttäväksi, mutta ei syövyttäväksi.
Vaikka monet arkisetkin aineet luetellaan laimentamattomana ärsyttäväksi tai jopa syövyttäväksi, “H361, epäilty lisääntymistoksisuus” voidaan katsoa vakavammaksi luokitukseksi. (Lähde: Sosiaali- ja terveysministeriö)
1.2. Aineen käyttö ihmisille
EU:n rehulisäainepaneeli FEEDAP huomauttaa, että Bovaer ei ole tarkoitettu ihmisten ruoan lisäaineeksi.
“Lisäksi FEEDAP-paneeli katsoi, että koska 3-NOP:n genotoksisuus ei ole täysin selvitetty, altistuminen lisäaineen hengitystiealtistukselle saattaa aiheuttaa lisäriskin lisäainetta käsittelevälle käyttäjälle.”
Johtopäätös
Aine on puhtaassa muodossa luokiteltu myrkylliseksi, mutta olennainen kysymys kuluttajien turvallisuuden kannalta on, siirtyykö aine lehmän kautta maitoon tai lihaan. Metaboliittien genotoksisuudesta on viitteitä, muttei täyttä selvyyttä ja sytotoksisuutta on todettu kokeissa. Tärkeää on myös lehmien turvallisuus.
2. Myrkyllisyys lehmille
Johdanto
Bovaer-lisäaineen kehittäjä DSM (nykyisin DSM-Firmenich) haki EU:lta lupaa tuotteen käytölle märehtijöiden rehussa. Hakemus siirrettiin arvioitavaksi Euroopan elintarviketurvallisuusvirastolle (EFSA).
EFSA ei siis suorittanut tutkimuksia itse, vaan arvioi DSM:n toimittamat aineistot.
“Saatujen tietojen arvo on kuitenkin rajallinen (esim. tutkimukset oli suunniteltu määrittämään aineen tehokkuutta), eikä niitä voida käyttää lisäaineen turvallisuuden todentamiseen märehtijöille.”
–EFSA, 3.2.4. Turvallisuus kohdelajille
EFSA totesi kaksi tutkimusta käyttökelpoisiksi turvallisuuden arvioimiseksi. Nämä tutkimukset olivat sietokokeita, joissa lypsylehmille annettiin arvioitavaa ainetta nousevina pitoisuuksina ja vaikutuksia mitattiin. Samoja tutkimuksia käyttivät arvioinneissaan myös Iso-Britannian ruokaturvallisuusvirasto FSA ja Japanin elintarviketurvallisuuskomissio FSCJ.
Turvallisuusarvio turvalliseksi hyväksytystä annostuksesta pohjautuu näihin kahteen tutkimukseen.
2.1. Myrkyllisyys lehmille suurilla annoksilla
Ensimmäinen tutkimus: EFSA:n arvioimassa tutkimuksessa 16 lehmää jaettiin neljään ryhmään, joille annettiin 3-NOP:a eri annosvahvuuksilla (0, 80, 400 tai 800 mg per kilo kuiva-ainetta) seosrehuun sekoitettuna.
Tutkimuksen tarkoitus oli selvittää siedettävä annosalue ja tunnistaa mahdollisia haittavaikutuksia eri annostasoilla.
“Kahdessa korkeimmassa annosryhmässä (400 ja 800 mg/kg) kaksi lehmää jouduttiin lopettamaan ennenaikaisesti, syönnin vähenemisen ja letargian vuoksi.”
Lähde: EFSA, 2021 (3.2.4.2.)
2.1.1. Tutkimuksessa havaitut muutokset
Suurempien 3-NOP-annosten ryhmässä havaittiin merkittäviä muutoksia:
- ruokahaluttomuutta (EFSA)
- letargiaa eli syvää väsymystä ja lamaantuneisuutta (EFSA)
- sydämen painon pienenemistä suurimmalla annoksella (FSCJ)
Muutokset viittaavat vakaviin elimistön ja aineenvaihdunnan häiriöihin.
2.1.2. Päätelmät tutkimuksesta
Vaikka otanta on rajallinen ja havainnot eivät suoraan todista, että muutokset johtuivat yksinomaan 3-NOP:sta, aineen vaikutusta voidaan pitää merkittävänä, sillä ilmiöt havaittiin toistuvasti korkeimmilla annostasoilla.
Vaikutusmekanismin arvioimiseksi ei ole saatavilla tarkempaa dataa, mutta havainnot viittaavat että suurilla annoksilla 3-NOP voi aiheuttaa vakaviakin terveysongelmia lehmille.
Johtopäätös: Tutkimuksen perusteella 3-NOP vaikuttaa olevan myrkyllinen lehmille suurilla annoksilla.
2.2. Myrkyllisyys lehmille suositusannoksilla
Toinen tutkimus: EFSA:n arvioimassa tutkimuksessa 80 Holstein-Friisiläistä lehmää jaettiin neljään ryhmään, joille annettiin 3-NOP:a eri annosvahvuuksilla (0, 80, 100 tai 200 mg per kilo kuiva-ainetta) seosrehuun sekoitettuna. Lehmien terveyttä ja aineenvaihduntaa seurattiin ja mitattiin 56 päivän ajan.
Tämä on merkittävin tutkimus turvallisen annostuksen hyväksymisessä.
FAKTA: Valmistajan suosittelema maksimiannos 3-NOP:a on 100mg/kg ja minimiannos 60mg/kg kuiva-ainetta.
2.2.1. Merkittävät havainnot toisesta tutkimuksesta
EFSA:n raportissa esitetyn taulukon perusteella lehmillä havaittiin mm. seuraavia muutoksia:
- Munasarjojen painon vähentymistä etenkin tupla-annoksella (tilastollisesti merkitsevä, n. 22-25% lasku suhteessa kontrolliin) ja mahdollinen trendi myös alemmissa annosryhmissä. Tämä voi olla merkki hormonitasapainon häiriöstä ja lisääntymiskyvyn heikkenemisestä. ¹ ²
- ALT-entsyymitasot laskivat jo alemmilla annoksilla. Tämä voi olla merkki maksan metabolian ja energiatuotannon muutoksista. ³
- Rehunkulutukseksen ja veden juonnin vähentymistä havaittiin tupla-annoksella (tilastollisesti merkitsevä). Tämä voi olla merkki aineenvaihdunnan muutoksista ja/tai energiatasapainon häiriöstä. ⁴
Mittaustulokset
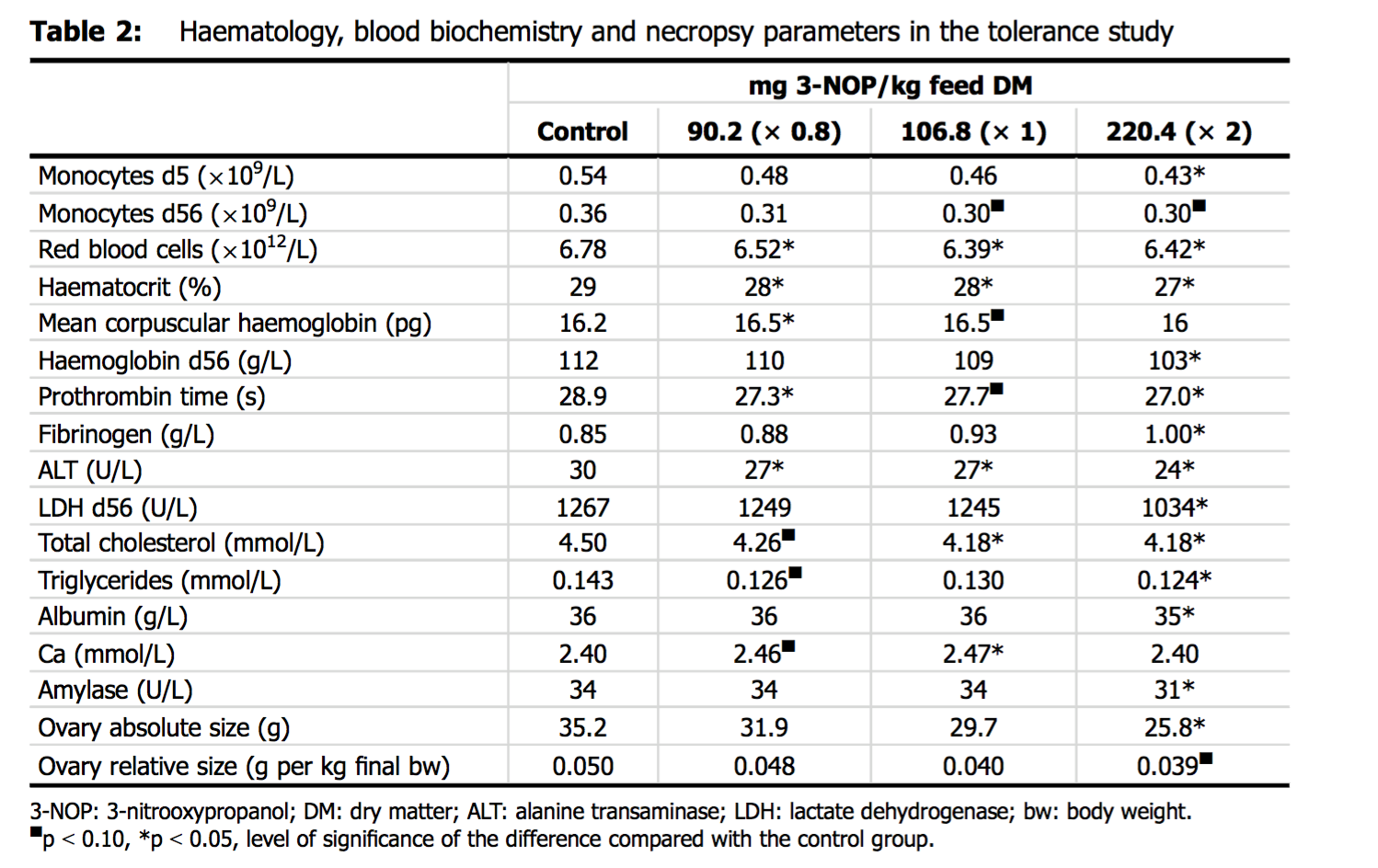
 (p < 0,10). Lähde: EFSA (3.2.4.2.)
(p < 0,10). Lähde: EFSA (3.2.4.2.) Tilastollisesti merkitseviä muutoksia havaittiin useissa fysiologisissa parametreissä eri 3-NOP -annostuksilla. Munasarjojen painon vähentymisessä trendinä näkyvä mahdollinen annosvaste antaa aihetta lisätutkimuksiin.
2.2.2. Lisääntymistoksisuus
“Merkittävät muutokset munasarjojen painossa kontrolliryhmään verrattuna tulisi tulkita merkkinä naaraiden lisääntymistoksisuudesta.”
Lähde: EPA, Lisääntymistoksisuuden riskiarviointiohjeistus 3.2.4.2.2.1.
Munasarjojen painon pieneneminen voi heikentää lehmien tiinehtimiskykyä.
2.2.3. EFSA:n arvio tutkimuksen tuloksista
EFSA arvioi useissa parametreissä havaittuja muutoksia “tilastollisesti merkittäväksi”, mutta “kliinisesti vähämerkityksisiksi”. Käytännössä siis selkeitä muutoksia elintoiminnoissa havaittiin, mutta niillä ei arvioitu olevan välitöntä haittaa eläinten terveydelle tai toimintakyvylle.
Näihän johtopäätöksiin päädyttiin, koska mitatut arvot pysyivät viitearvojen sisällä 56 päivän tutkimusjakson aikana eikä selkeitä histopatologisia muutoksia (kuten kudosvaurioita tai huomattavaa tulehdusta) havaittu.
2.2.4. Turvallisuusmarginaali
EFSA kuitenkin huomauttaa:
“Turvallisuusmarginaalia ei voitu määrittää.”
–EFSAYhteenveto turvallisuudesta kohdelajille (3.2.4.3.)
Toisin sanoen, haitattoman ja haitallisen annoksen välistä rajaa ei voitu määrittää, sillä kaikilla testatuilla annoksilla havaittiin muutoksia, eikä selkeää haitattoman annoksen tasoa voitu todentaa. Käytännössä tämä tarkoittaa, että on vaikeaa arvioida tarkasti, mikä annos on turvallinen ja mikä ei, erityisesti pitkäaikaisessa käytössä.
Johtopäätös myrkyllisyydestä lehmille:
- Havainnot viittaavat aineen mahdolliseen lisääntymistoksisuuteen
- Pitkän ajan turvallisuustutkimuksia lehmillä ei arvioitu
- Varovaisuusperiaatteen nimissä emme suosittele aineen käyttöä lehmillä.
3. Myrkyllisyys yleisesti (3-NOP)
Valmistaja toimitti myös muita tutkimuksia, joissa tutkittiin spesifisti eri menetelmillä myrkyllisyyden eri muotoja, kuten genotoksisuutta ja karsinogeenisuutta. Tulokset eläinkokeissa ja koeputkitesteissä olivat sekä positiivisia, että negatiivisia ja osittain epäselviä.
3.1. In vitro (koeputkessa)
Bakteerikokeissa ei havaittu merkittäviä vaikutuksia geenimutaatioden suhteen, vaikka testit tehtiin suurilla annoksilla. Ilman metabolista aktivointia suurin osa kokeista ei osoittanut merkittäviä haittavaikutuksia
Koeputkioloissa hamsterin soluilla ei aluksi huomattu kromosomivaurioita, mutta metabolisella aktivaatiolla havaittiin tilastollisesti merkittäviä mikrotumia, joiden analysoitiin sisältävän kromosomimurtumia. Paneeli totesi, että 3-NOP voi aiheuttaa kromosomivaurioita klastogeenisen vaikutusmekanismin kautta.
“Paneeli toteaa, että 3-NOP:n genotoksisuuspotentiaalia ei voi poissulkea.”
–EFSA
Mikrotumia havaittiin myös ihmisen lymfosyyteistä johdetuilla TK6-soluilla, vaikkakin hieman vähäisemmin. Koejärjestelyä ei kuitenkaan pidetty OECD:n ohjeistusten mukaisena, mikä saattoi alentaa tulosta.
Vaikka 3-NOP:lla havaittiin joitakin positiivisia löydöksiä genotoksisuuden osalta, on tärkeää huomata, että koeputki-testit eivät aina heijasta olosuhteita eliössä.
3.2. In vivo (eliöissä)
Kokeessa, joissa rotat altistettiin 3-NOP:lle, havaittiin vaikutuksia lisääntymiskykyyn. Vaikka suurilla annoksilla kaikki naaraat osoittivat parittelukäyttäytymistä, yksikään ei tullut raskaaksi ja yhdeltäkään ei löytynyt keltarauhasia tai alkion kiinnittymiskohtia. Uroksilla todettiin vakavaa heikkenemistä siittiöntuotannossa. Kahden vuoden karsinogeenisuustutkimuksessa raportoitiin hyvänlaatuisia mesenkymaalisia kasvaimia rotilla. Vaikka nämä eivät olleet tilastollisesti merkittäviä, niiden harvinaisuus viittasi löydösten merkityksellisyyteen.
Iso-Britannian ruokaturvallisuusvirasto FSA arvioi tutkimusta, jossa korkeimmalla annoksella rotilla havaittiin tilastollisesti merkittävä mikrotumien lisääntyminen, mutta tulos jäi kontrollirajojen sisälle. OECD:n ohjeistuksen mukaan epäselvässä tapauksessa vaaditaan lisätutkimusta. Valmistajan (DSM) palkkaama ulkoinen konsultti arvioi lisäyksen johtuneen Giemsa-värjäyksen aiheuttamasta artefaktista eli värjäysvirheestä näytteessä. Tämän perusteella FSA:n paneeli totesi 3-NOP:n olevan ei-genotoksinen in vivo -olosuhteissa. EFSA arvioi saman kokeen tuloksen epäselväksi.
EFSA:n raportissa mainitaan myös koirakoe, jossa ei muuten havaittu merkittäviä muutoksia, mutta yksi naaraskoira sai äkillisesti vakavia oireita kuten kävelyvaikeuksia, letargiaa ja epileptisiä kohtauksia. Kyseisen eläimen verenkierrossa 3-NOP:n aineenvaihduntatuotteen, NOPA:n, pitoisuus oli korkea ja laski hitaasti. Syy oli tuntematon.
VÄITE 3
HAJOAMINEN
“Aine hajoaa märehtijän pötsissä eikä sitä siirry maitoon tai lihaan.“
TARKISTUS: Osittain väärin.
Johdanto
Pötsi on märehtijöiden ruoansulatusjärjestelmän keskus, jossa bakteerit hajottavat kuitupitoisia kasveja ja muuntavat ne hyödynnettäviksi ravinteiksi. Se on miljoonien vuosien aikana kehittynyt ainutlaatuinen järjestelmä ja mahdollistaa sellaisten kasvien hyödyntämisen, joita muut eläimet eivät voi sulattaa.
Pötsissä vallitseva herkkä tasapaino vaikuttaa suoraan eläimen terveyteen ja siihen, kuinka hyvin ravinteet päätyvät maidoksi ja lihaksi. Erityisesti arkkibakteerit ovat tärkeitä, koska osa mikrobeista tuottaa vetyä, joka voi häiritä muita fermentaatioprosesseja, jos sitä kertyy liikaa. Arkkibakteerit käyttävät vetyä ja tuottavat samalla metaania ylläpitäen ruoansulatuksen tasapainoa.
FAKTA: 3-NOP estää metanogeenisten arkkibakteerien MCR-entsyymin toimintaa. Lisääntynyt vedyn määrä pötsissä vaikuttaa lehmän aineenvaihduntaan.
1. Hajoaako aine pötsissä?
3-NOP metaboloituu märehtijän pötsissä useiksi aineenvaihduntatuotteiksi, kuten NOPA:ksi (3-nitroksipropionihappo), nitraatiksi, nitriitiksi ja 1,3-propaanidioliksi.
NOPA-metaboliittia on havaittu myös lehmien verenkierrossa (plasmassa 65–104 µg/kg). Tämä osoittaa, että 3-NOP ei täysin hajoa pötsissä, vaan sen aineenvaihduntatuotteet pääsevät verenkiertoon ja voivat kulkeutua muualle kehoon ja maitoon.
2. Päätyykö metaboliitteja maitoon tai lihaan?
Jos aineenvaihduntatuotteet päätyvät verenkiertoon, niitä voi päätyä myös kudoksiin ja maitoon.
2.1. NOPA
3-NOP:n aineenvaihduntatuotteen NOPA:n jäämien arvioinnissa EFSA käytti kahta samaa tutkimusta kuin annoksen määrittelyssä (ks. VÄITE 2). Toinen tutkimuksista hylättiin tässä yhteydessä pienen otannan vuoksi (16 lehmää). Arviossa tarkasteltiin 56 päivän tutkimusta, jossa oli 20 lehmää kolmessa annosryhmässä (80mg, 100mg ja 200mg per kilo kuiva-ainetta).
NOPA-pitoisuus maidossa eri ryhmillä Ryhmä 1, 80 mg: -15 lehmän maidossa alle 1 µg/kg. -2 lehmän maidossa 1,11–2,51 µg/kg. -3 lehmän tiedot ei saatavilla. Ryhmä 2, 100 mg: -12 lehmän alle 1 µg/kg. -7 lehmän maidossa yli 1 µg/kg. -1 lehmän tiedot ei saatavilla. Ryhmä 3, 200 mg: -Korkein mitattu 3,66 µg/kg. -Muita tietoja ei saatavilla. Mittausraja: 1 µg/kg Lähde: EFSA (3.2.2.)
Tulokset
- NOPA:a havaittiin maidossa vaihtelevina pitoisuuksina, mutta määrät olivat vähäisiä
- NOPA:a ei havaittu kudoksissa tai lihassa määrinä, jotka mittausmenetelmillä voitaisiin varmuudella todentaa (alle 5 µg/kg)
Myös FSA (Iso-Britannia) ja FSCJ (Japani) tekivät arvionsa näiden kahden valmistajan lähettämän tutkimuksen perusteella.
“Pitoisuuden havaittiin kasvavan annosmäärän ja ajan myötä.”
Tämä ei kuitenkaan automaattisesti tarkoita, että vaikutus olisi merkittävä tai haitallinen.
NOPA:lla on kuitenkin havaittu joitain genotoksisuuteen viittaavia ominaisuuksia (ks. Väite 4).
Genotoksisille aineille turvallista minimiannostusta ei voida määritellä.
2.2. Hiilirakenteiden siirtyminen
EFSA:n mukaan 3-NOP:n hiilirakenteet päätyvät enimmäkseen uloshengitettävään hiilidioksidiin, maidon laktoosiin, lihan proteiineihin tai rasvahappoihin. Tämä tarkoittaa, että aineen hajottua sen osia käytetään osana normaalia aineenvaihduntaa, eli 3-NOP muuttuu aineenvaihdunnassa enimmäkseen elimistön tavallisiksi ainesosiksi, kuten hiilidioksidiksi, laktoosiksi ja proteiineiksi jne. Tämän ei uskota yleisesti olevan vaarallista. Tulos mitattiin lisäämällä radioaktiivista hiiltä 3-NOP:in ja seuraamalla sen kulkua elimistössä.
2.3. Mahdolliset tuntemattomat metaboliitit
Tanskan elintarvike- ja maatalouskeskuksen katsauksessa on myös esitetty mahdollisena riskinä, että 3-NOP:n aineenvaihdunta saattaa tuottaa tuntemattomia metaboliitteja.
Johtopäätös:
- Väite, että 3-NOP hajoaa kokonaan, eikä siirry maitoon tai lihaan, on osittain väärin.
- Aine metaboloituu pötsissä, mutta voi siirtyä verenkiertoon.
- NOPA-metaboliittia on havaittu maidossa, vaikkakin pieninä pitoisuuksina.
VÄITE 4
VAARALLISUUS
“Lypsylehmien metaanipäästöjä vähentävä rehun lisäaine hajoaa pötsissä eikä ole tutkimusten mukaan vaarallinen.“
TARKISTUS: Väärin.
Päivitykset:
-25.12.2024 väite uudelleentarkistettu.
-3.1.2025 päivitetty tietoja NOPA:n rakennetta koskien ja lisätty Ruokaviraston vastaus kohtaan 1.2.
-31.1. täsmennetty sytotoksisuus-havaintoa ja genotoksisuuden arviointia kohdassa 1.1.1. sekä lisätty Tukesin vastaus kohtaan 1.2.
1. Vaarallisuusriski ihmisille
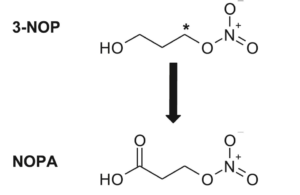
Johdanto
3-NOP metabolisoituu mm. 3-nitroksipropionihapoksi (NOPA). Vaikka se ei ole varsinainen nitro-yhdiste, havainnot (kuten positiivinen AMES-testi, lähde: EFSA) viittaavat siihen, että NOPA:lla voi olla DNA:ta vahingoittavaa potentiaalia. Tämän vuoksi genotoksisuuteen on syytä kiinnittää erityistä huomiota.
- Genotoksisuus tarkoittaa aineen kykyä vahingoittaa solujen perimää, kuten DNA:ta, joko suoraan tai epäsuorasti. Genotoksiset aineet voivat aiheuttaa DNA-vaurioita, jotka voivat puolestaan johtaa mm. mutaatioihin, solukuolemiin, kudosvaurioihin, syövän kehittymiseen, hedelmällisyyden heikkenemiseen tai perinnöllisiin sairauksiin, samalla heikentäen elinten normaalia toimintaa ja kudosten uusiutumista.
Pitkällä aikavälillä, erityisesti pienten annosten kohdalla, vaikutukset voivat pysyä piilossa vuosien ajan. Vauriot voivat kuitenkin kumuloitua, ilman havaittavia oireita, kunnes tietty kynnys ylittyy.
Jatkuva altistus genotoksiselle tai sytotoksiselle aineelle, pienissäkin määrin, voi aiheuttaa kaskadivaikutuksen, missä tietyn pisteen jälkeen vauriot alkavat kumuloitua nopeammin kuin elimistön korjausmekanismit ehtivät korjata niitä. Tämän jälkeen voi ilmetä äkillisiä ja vakavia seurauksia.
Genotoksisille aineille ei voida varmuudella määrittää turvallista annosta tai kynnysarvoa, ja ne vaativat erityistä varovaisuutta. Tämä tekee pitkän aikavälin riskiarvioinnista ja mahdollisten riskien minimoimisesta erityisen tärkeää.
1.1. NOPA-metaboliitin genotoksisuus
3-NOP:n aineenvaihdunnan tuloksena muodostuu 3-nitroksipropionihappoa (NOPA), jonka mahdollisia vaikutuksia DNA:han on tutkittu laboratorio-olosuhteissa. Erityisesti AMES-testissä havaitut pistemutaatiot osoittavat, että NOPA voi potentiaalisesti vahingoittaa perimäainesta. Tämän vuoksi NOPA:n genotoksisuutta on perusteltua tarkastella systemaattisesti ja varovaisuusperiaatteeseen nojaten.
1.1.1. NOPA:n genotoksisuusarviointi
NOPA:n genotoksisuutta tutkittiin neljällä spesifillä kokeella, joiden tulosten perusteella voidaan pyrkiä päättelemään aineen mahdollista genotoksisuutta.
- Testi 1: Bakteerikokeissa (AMES-testit) NOPA aiheutti geenimutaatioita (pistemutaatiot) kahdessa bakteerikannassa, sekä metabolisella aktivaatiolla että ilman. Tämä tarkoittaa, että aine voi aiheuttaa DNA-vaurioita joko suoraan tai aineenvaihdunnan kautta aktivoituna, mikä viittaa genotoksisuuteen.
- Testi 2: Ihmisen lymfosyyteillä suoritetussa kokeessa NOPA ei lisännyt merkittävästi mikrotumien esiintymistiheyttä koeputkioloissa. Tulos ei kuitenkaan sulje pois genotoksisuuden mahdollisuutta muilla mekanismeilla (esim. sytotoksisuuden epäsuorat vaikutukset tai epigeneettiset muutokset), sillä tämän tyyppinen testi ei tunnista kaikkia DNA-vaurioiden mekanismeja.
- Testi 3: Rottakokeessa ei havaittu mutaatioita cII-geenissä maksassa tai pohjukaissuolessa. Kuitenkin havaitut kliiniset oireet viittaavat siihen, että aine voi aiheuttaa toksisia tai sytotoksisia vaikutuksia, kuten elinten toiminnan häiriöitä. Tämä voi tarkoittaa, että aineen toksisuus ei rajoitu pelkästään genotoksisiin vaikutuksiin. Testi mittasi vain spesifisiä mutaatioita, eikä se arvioinut kumulatiivisia DNA-vaurioita tai muita mekanismeja, jotka eivät suoraan ilmene mutaatioina.
- Testi 4: Samassa koeasettelussa testattiin myös mikrotumien lisääntymistä, mutta niitä ei havaittu merkittävästi. Kuitenkin merkittävä nuorten punasolujen väheneminen uroksilla osoitti sytotoksisuutta. Suoria mutaatioita ei havaittu tässä testissä, mutta sytotoksisuus viittaa siihen, että aine voi vaikuttaa solujen toimintaan tuhoavasti.
1.1.2. Akuutti suuri annostus vs jatkuva pitkäaikainen altistus
Akuutti, suuri annos voi myös olla niin toksinen, että vaikutukset kohdistuvat laajempiin solun mekanismeihin (esim. sytotoksisuus) ennen kuin spesifisiä geneettisiä muutoksia ehtii syntyä tai kumuloitua. Pitkän ajan karsinogeenisuustutkimuksia NOPA:lla ei ole tehty.
3-NOP:n ja sen metaboliittien vaikutuksista tai kertymisestä ihmisiin ei myöskään ole tarkkaa tietoa. EFSA ei pidä kumuloitumista todennäköisenä, mutta ilmoittaa että täyttä varmuutta asiasta ei ole. On myös huomattava, että vaikka itse aine ei kumuloituisikaan, sen vaikutus saattaa pitkällä aikavälillä kumuloitua.
Vuoden kestäneessä, 3-NOP:n kroonista toksisuutta mittaavassa rottakokeessa, NOPA:n todettiin aiheuttavan kiveksille toksisia vaikutuksia. Suuremmilla annoksilla kaikilla uroksilla havaittiin kivesten surkastumista ja epänormaaleja soluja sekä merkittävää siittiöiden liikkuvuuden ja määrän vähenemistä. Tutkimuksessa havaittiin, että 3-NOP:n hajoamistuote, NOPA, oli se metaboliitti, joka aiheutti nämä toksiset vaikutukset. Muutokset olivat pysyviä.
Pienelläkin päivittäisellä annoksella, jatkuva altistus, potentiaalisesti genotoksiselle tai sytotoksiselle aineelle voi kasvattaa kaskadivaikutuksen riskiä. Riski kasvaa, jos elimistön DNA:n korjauskyky on heikentynyt esimerkiksi ikääntymisen tai perinnöllisten tekijöiden vuoksi tai jos aineen vaikutus kohdistuu herkästi vaurioituviin kudoksiin.
Johtopäätös NOPA:n genotoksisuudesta
Vaikka geenimutaatioita ei ole kaikissa kokeissa havaittu, AMES-kokeiden positiiviset tulokset, havaittu sytotoksisuuteen viittaava retikulosyyttien vähentyminen (TG 474) ja kliiniset oireet viittaavat siihen, että saatavilla olevan tiedon perusteella NOPA on todennäköisesti sytotoksinen ja voi aiheuttaa soluvaurioita, mutta genotoksisuuttakaan, eli sen mahdollisuutta aiheuttaa vaurioita perimään, ei voida täysin poissulkea.
1.2. Genotoksisuuden riski ihmisille
EFSA arvioi että genotoksisuus ei olisi ihmisille merkittävä riski käytännön annostasolla, sillä märehtijöillä NOPA:n määrät ovat hyväksytyissä olosuhteissa hyvin pieniä.
- EFSA arvioi ihmisten mahdollisen altistumismäärän NOPA:lle laskelmana, joka perustui jäämätutkimuksiin lehmillä ja rottakokeista johdettuun hyväksyttävään päiväsaantiin (ADI-arvoon).
- EFSA on määrittänyt 3-NOP:n NOAEL-arvoksi (No Observed Adverse Effect Level), eli annostasoksi, jolla ei havaita haitallisia vaikutuksia, kolmasosan siitä annoksesta, joka aiheutti haittavaikutuksia rottakokeissa.
- Tämän arvion pohjalta laskettiin myös ADI-arvo (Acceptable Daily Intake), eli ihmisille hyväksyttävä päiväsaanti. EFSA laajensi tämän arvion koskemaan myös NOPA:a
Tärkeää on tiedostaa, että genotoksisille aineille ei voida määrittää turvallista annosta ja NOPA on osoittanut joitain viitteitä genotoksisuudesta, sytotoksisuuteen viittaavien vaikutusten lisäksi.
Tiedustelimme Tukesilta (Turvallisuus- ja kemikaalivirasto) ja Ruokavirastolta, miten varovaisuusperiaatetta tulee soveltaa aineen suhteen, jonka genotoksisuudesta ei ole yksiselitteistä varmuutta.
Tukesin mukaan positiivinen Ames-testi viittaa genotoksisuuden mahdollisuuteen, mutta negatiiviset in vitro ja in vivo mikrotumatestit vähentävät kromosomivaurioiden todennäköisyyttä. Elintarviketurvallisuudesta vastaa Ruokavirasto.
“Yleisesti ottaen varovaisuusperiaatteen mukaisesti myös epäiltyjä genotoksisia karsinogeeneja tulisi kohdella elintarvikeketjussa genotoksisten karsinogeenien tavoin. Asetuksen (EY) N:o 178/2002 14 artiklan mukaan elintarvikkeet, joita ei pidetä turvallisena, tulee vetää pois markkinoilta elintarvikealan toimijan toimesta saman asetuksen 19 artiklan mukaisesti.”
–Ruokavirasto
Mikäli NOPA aiheuttaisi DNA-vaurioita jatkuvasti pienillä pitoisuuksilla, solujen korjausmekanismit voivat ajan mittaan ylikuormittua, mikä voi johtaa vaurioiden kumuloitumiseen ja myös mutaatioiden syntymiseen.
Johtopäätös vaarallisuudesta ihmisille
Aineen metaboliittien vaikutuksia ihmisiin, erityisesti toistuvan ja jatkuvan matala-annosaltistuksen osalta, ei voida varmuudella määrittää, sillä ihmisillä ei ole tehty kokeita.
Aineen vaikutukset ihmisravinnossa jäävät näin ollen avoimiksi, mutta varovaisuusperiaatteen nimissä aineen päätymistä ruokaketjuun ei voi suositella.
2. Vaarallisuusriski lehmille
3-NOP vaikuttaa lehmän elimistössä suoraan ja epäsuorasti. Potentiaalisen toksisuuden lisäksi pötsin käymisprosessien muutokset voivat vaikuttaa merkittävästi lehmän hyvinvointiin.
2.1. Muutokset käymisprosesseissa
Merkittävin vaikutus pötsissä on vedyn lisääntyminen, kun vetyä käyttävien arkkibakteerien toiminta estyy. Tällöin vety etsii uusia reittejä, mikä vaikuttaa pötsin käymisprosessiin ja aineenvaihduntaan, erityisesti propionaatin lisääntymiseen ja asetaatin vähenemiseen.
Tästä voi seurata:
- Kuiva-aineen saannin laskua ja energia-aineenvaihdunnan muutoksia:
Muutokset pötsin toiminnassa voivat heikentää lehmän ruokahalua ja rehunkulutusta, sekä muuttaa energian tuotantoa elimistössä - Mikrobiomin tasapainon häiriöitä:
Vedyn ohjautuminen propionihapon tuotantoon vähentää etikkahapon muodostusta ja voi heikentää pötsin toimintaa - Maidon rasvahappokoostumuksen muutoksia ja lievää rasvapitoisuuden nousua
Propionihapon suhteellisen määrän kasvu aiheuttaa muutoksia maidontuotannossa
2.2. Syönnin väheneminen
Syönnin väheneminen ei ole yksiselitteistä, eikä sitä ole havaittu kaikissa tutkimuksissa tilastollisesti merkittävästi. 15 tutkimuksen meta-analyysi kuitenkin osoitti systemaattista rehun syönnin vähentymistä.
Tanskan elintarvike- ja maatalouskeskuksen katsauksen mukaan päivittäisen syönnin väheneminen voi johtua pötsin aineenvaihdunnan häiriöistä lisääntyneen vedyn takia tai rehun maittavuuden laskusta, mutta syitä ei täysin tunneta.
“Rehun syönnin väheneminen on tyypillinen sairauden merkki (Millman, 2007; Weary et al., 2009), ja se herättää huolta mahdollisista negatiivisista vaikutuksista eläinten hyvinvointiin.”
Lähde: Aarhusin yliopiston tutkimus
Johtopäätös:
- 3-NOP:lla ja NOPA:lla on havaittu spesifejä toksisia vaikutuksia eläinkokeissa
- Näiden kemikaalien genotoksisuutta ei voida poissulkea ja sytotoksisuutta on todettu
- Metaboliittien vaikutuksesta ihmisten terveyteen ei ole tutkimuksia tai tietoa
- Varovaisuusperiaatetta tulisi noudattaa riskiarvioissa
- Lehmillä pötsin käymisprosessien häiriöt ja vetyreittien muutokset voivat heikentää lehmien hyvinvointia.
VÄITE 5
TURVALLISUUS
“EFSA on siis todennut Bovaerin turvalliseksi sekä lehmille että ihmisille. Samaan lopputulokseen on päätynyt Britannian Food Standards Agency sekä Yhdysvaltain elintarvike- ja lääkevirasto FDA.“
TARKISTUS: Totta, mutta harhaanjohtavaa.
1. Turvallisuusarvio
EFSA, FSA ja FDA eivät ole todenneet Bovaeria täysin turvalliseksi, vaan arvioineet, että sitä voidaan käyttää turvallisesti vain tarkasti määritellyissä olosuhteissa ja annosrajoissa.
Aineen valmistaja DSM toimitti EFSA:lle kaksi lehmillä tehtyä turvallisuustutkimusta, joiden perusteella tehtiin hyväksyntää puoltava arvio turvallisesta enimmäisannostuksesta. Tutkimusten otannat olivat 16 sekä 80 lehmää ja molemmissa havaittiin haittavaikutuksia. Samat tutkimukset toimitettiin FSA:lle, joka hylkäsi toisen näistä tutkimuksista, koska otanta oli rajallinen ja kaksi koe-eläintä lopetettiin ennenaikaisesti. FDA:n arvioimista tutkimuksista ei ole tarkempia tietoja saatavilla.
Pitkän aikavälin turvallisuusdataa aineen epäsuorista vaikutuksista ihmisille ei myöskään ole olemassa.
1.1. Turvallisuusmarginaali
EFSA ei pystynyt määrittämään 3-NOP:lle turvallisuusmarginaalia, koska toleranssitutkimuksessa havaittiin vaikutuksia kaikilla testatuilla annoksilla. Tämä tarkoittaa, että turvallista rajaa haittavaikutuksille ei voitu todeta.
“Turvamarginaalia ei voitu määrittää. Tästä syystä FEEDAP-paneeli ei pysty tekemään johtopäätöstä Bovaer® 10:n turvallisesta ravitsemuksellisesta pitoisuudesta muiden märehtijälajien tai -kategorioiden osalta.”
Lähde: EFSA
VÄITE 6
LUOKITTELU
“EU:n rehun lisäaineista annetun asetuksen mukaan eläinten ruokinnassa saa käyttää vain hyväksyttyjä rehun lisäaineita, ja 3-NOP on tällainen hyväksytty lisäaine.“
TARKISTUS: Totta.
1. Hyväksytyt rehun lisäaineet
Rehun lisäaineen käyttö vaatii hyväksynnän (Rehulisäaineasetus 3 artikla 1.b). 3-NOP on hyväksytty EU:ssa rehun lisäaineeksi, mutta sen käyttö on tarkoin säädelty tietyillä rajoituksilla.
Rehulisäasetuksen mukaan lisäaineen on yleensä parannettava rehun tai eläintuotteiden ominaisuuksia, kuten rehun koostumusta, säilyvyyttä tai aistinvaraisia ominaisuuksia. Poikkeuksena on kuitenkin kohta, joka sallii lisäaineet, joiden pääasiallinen tarkoitus on vähentää tuotannon ympäristövaikutuksia (5 artikla 3. e).
2. Lisäaine vai lääkeaine?
Yhdysvaltojen lääkelain mukaan Bovaer on lääke, sillä se on tarkoitettu vaikuttamaan eläimen kehon elintoimintoihin tai rakenteeseen. FDA:n eläinlääkekeskus (CVM) ei aio kuitenkaan valvoa sen lääkevaatimuksia.
“Vaikka Bovaer® 10 on hyväksymätön lääke, emme tällä hetkellä aio ryhtyä täytäntöönpanotoimiin yllä mainittujen lääkevaatimusten osalta.”
FDA:n eläinlääkekeskus (CVM) 24.5. 2024
2.1. EU-laki eläinlääkinnästä ja rehulisäaineista
Kysyimme Euroopan lääkevirastolta (EMA), voiko farmakologista ainetta, joka vaikuttaa spesifisesti eläimen elintoimintoihin, pitää EU-lainsäädännön mukaan eläinlääkkeenä. EMA:n mukaan Euroopan eläinlääkeasetuksen (Artikla 4) määritelmän mukaan ei, koska sen tarkoituksena ei ole sairauden hoito. Lääkevirasto neuvoi olemaan yhteydessä kansallisiin viranomaisiin.
2.2. Suomen lääkelaki
Suomen lääkelain mukaan lääkeaine määritellään seuraavasti:
“Lääkeaine on kemiallisesti tai muuten tieteellisin menetelmin yksityiskohtaisesti määritelty elimistöön vaikuttava aine, jota käytetään lääkevalmisteen valmistuksessa tai lääkkeenä sellaisenaan.
– Lääkelaki 5 §
Tämän määritelmän mukaan 3-NOP luokiteltaisiin lääkeaineeksi, koska se vaikuttaa kohdelajin elimistöön estämällä spesifin entsyymin (MCR) toimintaa. Eläinten lääkitsemistä koskevan lain mukaan (7 § ) lääkkeitä tulee Suomessa käyttää niin, että ne edistävät eläimen terveyttä ja hyvinvointia.
2.3 Hyväksymisprosessi Suomessa
3-NOP ei ole saanut Suomessa erillistä kansallista hyväksyntää, vaan se on otettu käyttöön osana Suomen lainsäädäntöä EU:n suoran sovellettavuuden periaatteen mukaisesti.
Tämä tarkoittaa, että EU:n komission päätös tuli suoraan voimaan Suomessa ilman erillistä kansallista päätöstä tai että kansalliset päättäjät käsittelivät tai edes tiedostivat asiaa aktiivisesti. (Rehulaki, 9 §). Tätä käytäntöä kutsutaan viittaustekniikaksi, ja sen kautta Bovaer-rehulisäaine on hyväksytty automaattisesti myös Suomessa.
VÄITE 7
HYVÄKSYMISPROSESSI
“Se, pääseekö rehun lisäaine hyväksyttyjen listalle, riippuu siitä, onko se turvallinen eläimille, ihmisille ja ympäristölle, ja lisäksi arvioidaan sen tehokkuutta.“
TARKISTUS: Osittain väärin.
1. Hyväksyminen listalle
On totta, että EU-lain mukaan rehulisäaineet eivät saa olla haitallisia.
“Rehun lisäaine ei saa vaikuttaa haitallisesti eläinten tai ihmisten terveyteen tai ympäristöön.”
Rehun lisäaineiden hyväksyntäprosessi ei ole kuitenkaan yksiselitteinen turvallisuuden tae.
Päätöksen tekee Euroopan komissio, joka perustaa ratkaisunsa EFSA:n lausuntoon.
Faktabaarin artikkelissa haastateltu Tarja Root Ruokaviraston rehuvalvonnasta kuvaa prosessia:
“EFSA:n lausunnon perusteella komissio valmistelee yhdessä jäsenvaltioiden kanssa rehun lisäaineen hyväksynnän ja julkaisee sen toimeenpanoasetuksena.”
–Tarja Root, Ruokaviraston rehuvalvonta
2. Turvallisuusarviointiprosessi
Komissio pyysi EFSA:lta arvion 3-NOP:n turvallisuudesta ja tehokkuudesta.
Arvio turvallisesta annostuksesta perustui kahteen tutkimukseen lehmillä. EFSA:n oman ohjeistuksen mukaan vastaavien tutkimusten tarkoitus on arvioida toksisuutta kohdelajille ja löytää turvallisuusmarginaali.
“Toleranssitutkimuksen tavoitteena on antaa rajallinen arvio lisäaineen lyhytaikaisesta toksisuudesta ja sen turvallisuusmarginaalista kohde-eläimille.”
EFSA, Opas rehun lisäaineiden turvallisuuden arvioimiseksi kohdelajeille, 2017b
Tämän turvalliseksi katsotun annostuksen mukaan arvioitiin myös ihmisten altistusriskiä.
2.1. Turvallisuusarvioinnin rajoitteet
EFSA arvioi kahta tutkimusta aineen annostelun ja mahdollisten haittavaikutusten määrittämiseksi. Tutkimuksissa ilmeni biologisesti merkittäviä muutoksia, kuten elinten painon pienenemistä.
EFSA raportoi että turvallisuusmarginaalia ei voitu määrittää 3-NOP:lle.
OECD:n (Taloudellisen yhteistyön ja kehityksen järjestö) ja EPA:n (Yhdysvaltain ympäristönsuojeluvirasto) ohjeistukset korostavat, että elinten painonmuutokset voivat olla merkittäviä viitteitä toksikologisista vaikutuksista. Kansainvälisten arviointikäytäntöjen ohjaaja, OECD, ohjeistaakin tekemään pitkäaikaistutkimuksia, jos lyhytaikaisista kokeista ilmenee epäselviä tai huolestuttavia tuloksia. Tässä tapauksessa pitkäaikaistutkimuksia ei kuitenkaan tehty, vaikka löydösten vakavuus olisi niitä edellyttänyt.
Onkin oleellista huomata, että EFSA:n lausunto ei automaattisesti tarkoita aineen turvallisuutta, sillä prosessissa voi jäädä huomiotta olennaisia seikkoja. Tämä on erityisen merkittävää, koska julkisessa keskustelussa usein virheellisesti oletetaan, että virastojen hyväksymät aineet ovat aina täysin tutkittuja ja turvallisia.
Kysyimme OECD:ltä kantaa tämänkaltaiseen spesifiin tilanteeseen, missä tutkimuksessa havaitaan systemaattisia ja annosriippuvaisia muutoksia nk. apical endpoints -mittareissa (esim. elimen painossa), mutta histopatologisia muutoksia ei havaita. Tiedustelimme erityisesti, miten tällaisia havaintoja tulisi tulkita ja missä tilanteissa ne riittävät perusteeksi pitkäaikaistutkimusten tarpeelle tai tarkemman arvioinnin vaatimiseen. Odotamme vastausta. Asia luvattiin puhelimessa käsitellä nopeutetusti.
VÄITE 8
LUOMUTUOTANTO
“Luomutuotannossa Bovaeria ei saa käyttää.“
TARKISTUS: Totta.
Luomutuotteissa Bovaerin käyttö on kielletty.
Luomuliiton kotieläinasiantuntija Katarina Rehnström on todennut:
Luomutuotannossa sen [Bovaer] käyttö ei ole sallittua, eli luomumaitoa voi käyttää huoletta myös tältä osin.” – Katarina Rehnström
Lähde: Luomuliitto.fi
VÄITE 9
TEHOKKUUS
“3-NOP vähensi lehmien metaanintuotantoa myös suomalaisissa tutkimuksissa, vaikkakin vaikutus jäi pienemmäksi kuin aiemmin kerrottu 30 prosenttia. Metaaninvähennyspotentiaali oli suurempi seosrehuruokinnassa kuin erillisruokinnassa.“
TARKISTUS: Totta, mutta tärkeää tietoa jätetty mainitsematta.
1. Suomalaisissa olosuhteissa
Helsingin yliopiston vanhempi yliopistolehtori Tuomo Kokkonen kommentoi Luonnonvarakeskuksen, Helsingin yliopiston, Valion ja A-Rehun IRMA-hankkeen tutkimustuloksia, joissa tarkasteltiin 3-NOP:n vaikutusta lehmien metaanintuotantoon suomalaisissa olosuhteissa. Kokkosen mukaan:
- Seosrehuruokinnassa 3-NOP:n metaanituotantoa vähentävä vaikutus (21–24 %) jäi kirjallisuudessa esitettyä pienemmäksi (keskimäärin 30 %).
- Erillisruokinnassa lisäaineen teho oli seosrehuruokintaa pienempi (7–11 %).
- Erillisruokinnassa 3-NOP:in metaanin tuotantoa vähentävä vaikutus pötsissä kestää noin kaksi tuntia.
2. Erillis- ja seosruokinta
Johtopäätöksenä Tuomo Kokkonen ei suositellut 3-NOP:n käyttöä erillisruokinnassa heikon tehon vuoksi, vaan ohjaisi mahdollisen käytön seosrehutiloille.
“Tulosten perusteella 3-NOP vähentää metaanintuotantoa myös erillisruokinnassa, mutta vaikutuksen laimeuden vuoksi mahdollinen 3-NOP:n käyttö kannattaa ohjata seosrehutiloille.” –Tuomo Kokkonen
Luken mukaan erillisruokinnassa on puolet Suomen karjasta.
VÄITE 10
VAIKUTUS
“Valio on vuonna 2023 kertonut, ettei pilotissa havaittu mitään muutoksia tilojen tuottaman maidon määrässä, pitoisuudessa tai laadussa. Lisäaine ei siis vaikuttanut lehmien maidontuotantoon tai maidon koostumukseen.”
TARKISTUS: Osittain totta, osittain epävarmaa.
1. Maatilapilotti
Maatilapilotissa testattiin ainetta 40 suomalaisella lypsylehmätilalla, noin 3000 lehmällä.
1.1. Valion kertomaa
Valio tosiaan on ilmoittanut vuonna 2023 Maito ja me -sivullaan seuraavaa:
“Myös tilojen tuottaman maidon määrät, pitoisuudet ja laatu arvioitiin, eikä näissä tekijöissä havaittu mitään muutoksia verrattuna pilottia edeltävään tai sen jälkeiseen aikaan.”
Lähde: Maitojame.fi
1.2. Tutkimusdata
Väitettä ei voida varmistaa, sillä maatilapilotin tutkimusdata ei ole julkisesti saatavilla. Olemme olleet yhteydessä Luonnonvarakeskuksen tutkimusprofessori Marketta Rinteeseen, joka kertoi, ettei voi jakaa tarkempaa dataa, koska se on Valion omaisuutta. Hän ohjasi meidät Valion ilmastotiimin kehityspäällikkö Virpi Klingin puoleen, mutta useista yhteydenottoyrityksistä huolimatta emme saaneet häntä kiinni. Näin ollen väitettä ei voida vahvistaa eikä kumota.
Kuitenkin Luonnonvarakeskuksen, Helsingin yliopiston, A-Rehun ja Valion IRMA-hankkeessa esitettiin, että aiemmassa suomalaisessa tutkimuksessa 3-NOP:n käyttö rehussa vähensi lehmien syöntiä (3–9 %) ja energiakorjattua maidontuotantoa (EKM) (3–6 %).
2. Vaikutus maidontuotantoon
Tanskalaisessa tutkimuksessa havaittiin, että
- Maidon tuotanto väheni 11,7%
- Energiakorjatun maidon tuotannon määrä väheni 9,0%
- Kuiva-aineen saanti eli syöminen väheni 13,4%
- Metaanin tuotanto väheni 18%-23%
“Suurimpien DMI-vähennysten kohdalla syöntikäyttäytyminen muuttui: lehmät söivät useammin, mutta pienempiä aterioita, syöntinopeus hidastui ja ne yrittivät useammin päästä kiellettyihin ruokintapaikkoihin.”
Eräässä meta-analyysissä (14 tutkimusta, 18 koetta ja 55 käsittelyä) havaittiin että 3-NOP osoitti taipumusta vähentää maidontuotantoa. Toisaalta tietyissä tutkimuksissa maidon tuotanto ei ole merkittävästi muuttunut, mutta energiakorjatun maidon määrä on noussut lievästi rasvapitoisuuden kasvun myötä, kun vety ohjautuu uusiin aineenvaihduntareitteihin.
3. Maidon koostumuksen muutokset:
Muuttuneiden aineenvaihduntareittien pitkäaikaisvaikutuksia lehmän energiatuotantoon ja maidon laatuun ei tunneta. Rasvahappojen muutokset ja lisääntynyt ureapitoisuus voivat myös vaikuttaa maidon laatuun, mutta näiden suhteen on vaihteluita eri tutkimuksien välillä.
JOHTOPÄÄTÖS
Kaiken käytettävissä olevan tiedon perusteella Bovaer-lisäaineen pitkäaikaista turvallisuutta lehmille ja kuluttajille ei ole selvitetty riittävän kattavasti. Turvallisuusmarginaalia ei voitu määrittää aineen hyväksymisprosessissa, eli haitattoman ja haitallisen annoksen välinen raja on epäselvä, ja jo lyhyissä tutkimuksissa on havaittu merkittäviä muutoksia esimerkiksi lehmien lisääntymisfysiologiassa sekä rehunsyönnissä. Aineen metaboliittien pitkäaikaisvaikutuksista ja toksisuusprofiilista on edelleen puutteellisesti tietoa.
Alan toimijoiden on syytä tehdä perusteellinen riskiarvio aineen käytön suhteen, mahdollinen mainehaitta ja turvallisuustekijät huomioon ottaen. Lehmät ovat Suomen elintarvikehuollon keskeinen kulmakivi, joten varovaisuusperiaatteen noudattaminen on perusteltua.
Saatavilla olevan tiedon valossa ei ole vastuullista suositella Bovaer-lisäaineen käyttöä lehmien ruokinnassa.
PERUSTEET:
- Nauta on korvaamaton osa Suomen huoltovarmuutta ja ravintoketjua, joten riskiarvioissa tulee noudattaa korostettua varovaisuusperiaatetta.
- Suomessa ainetta ei ole erikseen hyväksytty ja se täyttää lääkeaineen määritelmän.
- Hyväksymisprosessi EU:ssa perustui kahteen tutkimukseen, joissa havaittiin merkittäviä haittoja.
- 3-NOP-kemikaalin pitkäaikaisturvallisuus eläimille ja kuluttajille on edelleen epäselvä.
- Hajoamistuotteiden kuluttajaturvallisuudesta ja pitkäaikaisvaikutuksista on merkittäviä tietovajeita
- Kemikaalin kokonaisvaikutus maidontuotannon laatuun on epäselvä, mutta muutoksia on havaittu.
- Kemikaali vaikuttaa potentiaalisesti haitallisesti lehmien tiinehtimiskykyyn.
LOPPUKANEETTI
Kansakunnan Tila pitää tärkeänä, että Bovaer-lisäaineen kaltaiset aiheet herättävät keskustelua Suomessa. Olemme sitoutuneet faktoihin perustuvaan yhteiskunnalliseen vuorovaikutukseen ja toivomme, että tämä faktantarkistus kannustaa lukijoita pohtimaan aihetta laajasti ja keskustelemaan siitä asiallisesti.
Päivitys (25.12.2024): Lisätty tietoa NOPA-metaboliitin genotoksisuuteen liittyen (Väite 4, Vaarallisuus).
Päivitys (3.1.2024):
-Lisätty Ruokaviraston vastaus varovaisuusperiaatteen soveltamisesta genotoksisuusepäilyissä (Väite 4, kohta 1.2.)
-Päivitetty NOPA:n rakenteeseen liittyviä tietoja (Väite 4, Johdanto ja kohta 1.1. ensimmäiset lauseet).
-Korvattu “kuivarehua” sanalla “kuiva-ainetta” (Väite 2, Myrkyllisyys: kohta 2).
Päivitys (31.1.): Tarkennettu “Myrkyllisyys lehmille suositusannoksilla” -kohtaa. Täsmennetty NOPA:n sytotoksisuushavaintoa ja genotoksisuusarviointia (Väite 4, kohdat 1.1. ja 1.2.) . Lisätty Tukesin vastaus. (Väite 4, kohta 1.2.) Muutettu “hiilirungon” rakenteet muotoon “hiilirakenteet” (Väite 3, kohta 2.2.).










turvallinen niin kuin korona rokote .Valio on yksi suomen roska firmoista
Ihmettelin jo nuorena, että miten ihmeessä meillä oli voivuoria, joista ei meinattu päästä eroon, mutta voi ei kaupassa ollut mitenkään edullista ja margariinia tuputettiin joka paikassa.
Valiolle maksettiin voista varastointipalkkioita ja voita myytiin polkuhintaan itänaapuriin.
Miksi jo silloin puhdas luonnontuote oli niiiiin vaarallista, ettei sitä saanut kotimaassa syödä?
Oliko pekkapuska hömppätutkimukset syynä silloin?
Onko kukaan toimittaja vielä kysynyt kauppaketjujen kantaa mahdollisesti vaarallisten tuotteiden myymisestä myymälöissään kuluttajille?
Onko kauppaketju vastuussa myymistään tuotteista? Vai voidaanko vastuuta sysätä tuotteen valmistajalle, vaikka tiedettäisiin tuotteen mahdollinen vaarallisuus?
Voidaanko kauppaketjuja vaatia selvittämään myymiensä tuotteiden ehdoton vaarattomuus?
Ja kenen on vastuu, jos osoittautuu, että kauppaketju on tietoisesti myynyt vaarallista tuotetta, joka aiheuttaa vaurioita kuluttajille?
Eli aine voi aiheuttaa haittavaikutuksia lehmille ja estää uusien lehmien syntymistä; sitä siirtyy maitoon metaboliitteina, jotka on mahdollisesti aiheuttaa syöpää tms, koko turvallisuusarvio on ollut hätäinen ja luokittelu kyseenalainen? Ja Suomeen koko hommaa ei ole edes hyväksytty vaan se on tullut automaattisesti ulkomailta, mutta riskeeraa mahdollisesti Suomen huoltovarmuutta ja ruokaketjua. Hmm…
Alkaako agendan tarkoitus selvitä?
Väestön vähentämisestä on kyse. Sitä tehdään pitkällä ajanjaksolla, ettei siihen havahduttaisi ennen kuin on liian myöhäistä.
Maito ja muut meijerituotteet pois, ja samalla loppuu lihantuotanto nautojen osalta. Ja possuista päästään eroon lintuinfluenssalla, kun vaan rokotellaan riittävästi.
Ja sitten tarjotaan keinolihaa tai hyönteisiä tilalle. Tai veganismisa, joka näännyttää ihmiset loppuun.
Tuttavani lupasi toimia koekaniinina Valion tuotteille. Kattelen nyt muutaman vuoden, ehkä viisi. Jos hän on vielä silloin terveenä ja hengissä niin voin ehkäpä harkita Valion tuotteita. Siihen asti Valio ja myös Atria boikotissa. Mukavaa kun meillä on näitä koekaniineja joukossamme.. niin kuin geenipiikin ottaneita, joilla nykyäån kaikennäköisiä terveyshuolia jotkut jo mullan alla. Onneksi en kokeillut sitäkään..
Mistä tietää mitä tässä pitäisi uskoa ja mihin luottaa? Sitten kun lukee asiasta muualla, niin siellä väitetään että bovaerista on tehty 150 eri luotettavaa tutkimusta ja sen on havaittu olevan turvallinen jne. Eli mielipide liittyy siihen kuka on asiasta kirjoittanut ja mikä hänen agendansa tai maailmankuvansa on? Kyllä mäkin oon tosi epäileväinen bovaerin suhteen enkä luota viranomaisiin ja tutkimuksiin (mukana aina raha, politiikka, eturistiriidat jne). Mutta voiko ikinä saada selville kuka jakaa oikeasti luotettavaa tietoa?
Suomessa aletaan valmistaa keinolihaa tänä vuonna Lappeenrannassa, Valio on osakkaana tässä hankkeessa.
https://www.tekniikkatalous.fi/uutiset/keinolihan-tuotanto-alkaa-2025-suomeen-maailman-suurin-tehdas-jossa-valmistetaan-naudanlihaa/089c3db7-1299-44fe-9c6c-14ba16d57fb2
https://www.talouselama.fi/uutiset/lappeenrantaan-rakennetaan-keinolihatehdas/b0aaf554-adf0-4d76-80f9-c97710454864
https://www.synbiopowerlabs.com/post/keinolihan-tuotannon-merkitt%C3%A4v%C3%A4-askel-otetaan-nyt-suomessa-lappeenrantaan-rakenteilla-oleva-laitos
Valio on ilmoittanut, ettei erikois-mustaleima emmentalia enää valmisteta kustannussyistä. Vuoden 2024 aikana a.o. tuotetta on ollut jonkin verran vielä saatavana, mutta sen laatu on muuttunut huonommaksi: Juustoheran määrä on vähentynyt, juustossa esiintyy paljon halkeamia ja maku ei ole enää ennallaan. Asiaa ei ole kai lainkaan tutkittu, mutta voiko olla, että Boaverin pienikin siirtyminen maitoon josta juusto tehdään, vaikuttaa juuston kypsymisen biokemiaan??? Lienee aika herkkää kemiaa aikaisempien vuosien kokemusten kun perusteella…